リン酸仮説:5.ペプチド,ヌクレオチドの伸長
プロトポリマーを成長させる反応のうち,転写・翻訳系の発生に繋がったと想定する反応を 3 種類ピックアップして再編する.
これらはヌクレオチドの 3'-OH上での反応である(それに相当するプロトポリマーの部位の反応である).
- ヌクレオチドを結合する反応(後の核酸伸長反応)
- ペプチジル基間のアミノリシス(後のペプチド伸長反応)
- アミノ酸を結合する反応(後のアミノアシル tRNA の生成)
「現代の生物が獲得している代謝経路や反応機構をできる限りそのまま利用」という,このディレクトリの原則に沿って考えてみた.
Before : 4.酵素活性の起源 Next : 6.ヌクレオチドの起源目次(ページ内リンク)
ペプチド,ヌクレオチドの伸長反応の制限
ヌクレオチド様構造の 3'-末での反応制御
ケース 1:3'-末が修飾されていない場合
ケース 2:3'-末がアミノアシル化されている場合
プロトポリマーの成長反応
ペプチド,ヌクレオチドの伸長反応の制限
ペプチド,ヌクレオチドの伸長反応が発生した当時はいずれの制限も緩かったと考えるが,可能な限り現代のシステムと共通性をもたせる.
そうするとどのような制限が付くのか考えてみた.
この段階では,リボースの 2'-位 と 3'-位 は明瞭に区別しなかった.
- ビルディングブロックは,リボース,リン酸,核酸塩基,およびアミノ酸とする
- プロトポリマーのヌクレオチド部分どうしの会合は,逆平行とする
- アミノ酸ドナーとなるプロトポリマーのアミノ酸は,リボースの 2'/3'-ヒドロキシ基とアミノ酸のカルボキシル基との結合(アミノアシル-tRNA と一致)
- アミノ酸アクセプターとなるプロトポリマーのペプチドは,リボースの 3'-ヒドロキシ基とペプチドのカルボキシル基との結合(ペプチジル-tRNA と一致)
- ペプチド部分の伸長方向は N-末→C-末とする
- ヌクレオチド部分の伸長方向は 5'→3'とする
- ヌクレオチド部の核酸塩基は塩基対の形成に関わる.酵素活性はペプチドが有する
- 遺伝コードとアミノ酸との対応関係は現代と同じ,または現代の対応関係の下位互換とする
- アミノ酸配列は,それがコード化される場合は塩基配列にコード化される
- コドン領域の伸長とペプチド部分の伸長とを協奏的に進行させることを可能とする
ヌクレオチド様構造の 3'-末での反応制御
化学進化の特定の段階で,反応を制御するメカニズムが発生しなければならない.
プロトポリマーでは,リボースの 2'/3'-位にヌクレオチドまたはペプチドが付加することになる.
ここでは,ポリヌクレオチドの 3'-末の状態で反応を制御するメカニズムを考えてみる.
例えば,
- ペプチジル化されている場合には,ペプチドを伸長させる際の基質となる:ヌクレオチド部は伸長できない
- アミノアシル化されている場合には,ペプチドを伸長させる際の求核剤となる:ヌクレオチド部は伸長できない
- 遊離の場合には,ヌクレオチドを伸長させる際の求核剤となる:ペプチドは伸長できない
- 2'/3'-OH 基がリン酸化されている場合には反応に関与しない:いくつかのヌクレオチド関連物質の2'/3'-OH がリン酸化されていることから.弱い主張である
ケース 1:3'-末が修飾されていない場合
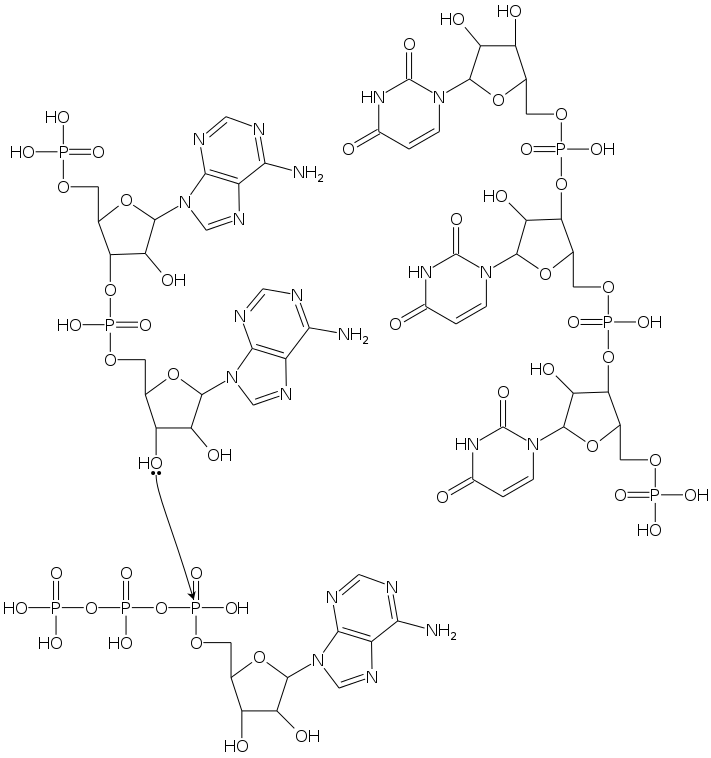
ヌクレオチドの伸長反応,あるいはリボースにアミノ酸を結合する反応の場を提供するとする.
画像には,テンプレートに依存してヌクレオチドが伸長する反応を描いた.
ポリヌクレオチド 3'-末が修飾されていない場合は,3'-O が求核剤となる.
- 求電子剤が,5'-OH がポリリン酸で活性化されたヌクレオチドのリン原子なら,ヌクレオチド様構造が伸長する
- 求電子剤が,カルボキシル基がポリリン酸で活性化されたアミノ酸のカルボニル炭素原子なら,アミノ酸を結合する反応となる
テンプレートに依存しない反応
テンプレートに依存しない反応では,基本的に核酸塩基がランダムなヌクレオチドが伸長する.
これは,単にヌクレオチド領域が伸長するだけであるが,化学進化のもっと後で遺伝子に相当する領域が拡大する反応ともみなせそうである.
ポリヌクレオチドをテンプレートにする場合
この反応が,画像のように,別分子のポリヌクレオチドをテンプレートにする場合は相補鎖が伸長する.
これは,転写,逆転写,および複製に繋がる反応である.
ケース 2:3'-末がアミノアシル化されている場合
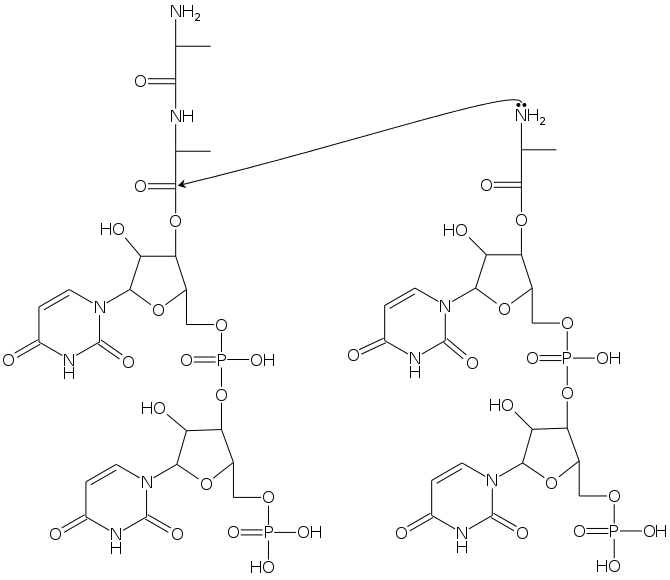
ペプチドの伸長反応の場を提供するとする.
上の画とは上下を反転して描いた.
ポリヌクレオチド 3'-末がアミノアシル化されている場合は,アミノアシル基の窒素原子が求核剤となる.
求電子剤は別分子の 3'-OH がペプチジル化されたヌクレオチドのカルボニル炭素である.
ペプチドの鎖長について
活性や特異性を上昇させるためには,ペプチドをある程度伸長させねばならない.
- 延長されるアミノ酸残基は 1 個とは限らない.ペプチドの融合・交換といったイメージである
- 融合されるペプチドが同様の活性(例えばリン酸捕獲活性)を有するなら,活性が向上するかも知れない
- 別種の活性(例えばリン酸捕獲活性と糖捕獲活性)を有するなら特異性の変化につながるかも知れない
特異性の萌芽?
ペプチドを構成するアミノ酸の性質の違いによって,そのプロトセルが含む構成成分に差異を生じるかもしれない.
- 塩基性アミノ酸が多いペプチドなら,プロトセルにリン酸誘導体が取り込まれ易くなる
- 酸性アミノ酸が多いペプチドなら,プロトセルに塩基性アミノ酸が取り込まれ易くなる
プロトポリマーの成長反応
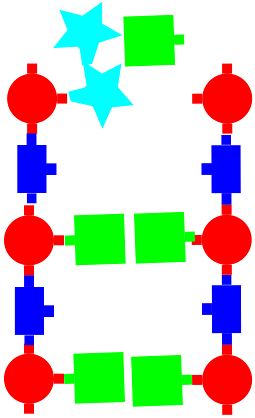
上の反応を外挿すると,こんな分子ができてしまうのではないか.
ここでは,プロトポリマーの末端に塩基を結合する反応を描いた.
塩基ではなく糖やリン酸,アミノ酸でも同じように描ける.
画像は,2 本のプロトポリマーが協奏的に成長するイメージである.
プロトポリマー間には,緑の正方形として描いた塩基対が 2 個生成しているように描いた.
向かって左のプロトポリマーはそのペプチド部分に核酸塩基を捕獲しており,向かって右のプロトポリマーの糖残基に核酸塩基を衝突させるところである.
プロトポリマーは,ペプチドと核酸塩基の両方を有するので次の機能を保有できる.
- プロトポリマーのペプチド残基は,特異的にビルディングブロックを捕獲する
- プロトポリマーの核酸塩基は,プロトポリマーどうしの会合に寄与する